
2021年5月24日,南方科技大学医学院助理教授田瑞琳与美国加州大学旧金山分校学者Martin Kampmann等在Nature Neuroscience发表研究文章“Genome-wide CRISPRi/a screens in human neurons link lysosomal failure to ferroptosis”,系统探究了人类神经元调节活性氧水平、应对氧化应激的机制,并意外地发现了一条神经元特异的铁死亡途径。
神经元作为人体内存活时间最久的末端分化细胞,在衰老过程中会受到许多细胞应激压力的胁迫,氧化应激(oxidative stress)是其中关键的一种。氧化应激是由于细胞内活性氧(reactive oxygen species, ROS)的过度积累所导致。过量的活性氧会导致DNA、蛋白质和脂质的损伤,引起细胞死亡。大脑对于活性氧格外敏感,因为大脑消耗大量氧气,具有丰富的高氧化还原活性的金属(如铁和铜)以及易受到活性氧损伤的多元非饱和脂肪酸,同时抗氧化因子数量相对有限。
许多研究表明,氧化应激参与到神经退行性疾病的发生。临床上,神经退行性疾病患者的大脑内活性氧水平升高,活性氧造成的损伤也增加。使用诱导多能干细胞模型的体外研究也证实,携带有神经退行性疾病基因突变的神经元氧化应激更加敏感。
为了找到神经元应对氧化应激所必需的通路,研究团队使用之前开发的在诱导多能干细胞(iPSC)分化的人类神经元中进行CRISPRi 筛选的技术,对神经元在正常条件和氧化应激条件下存活所必需的基因进行了全基因组筛选。
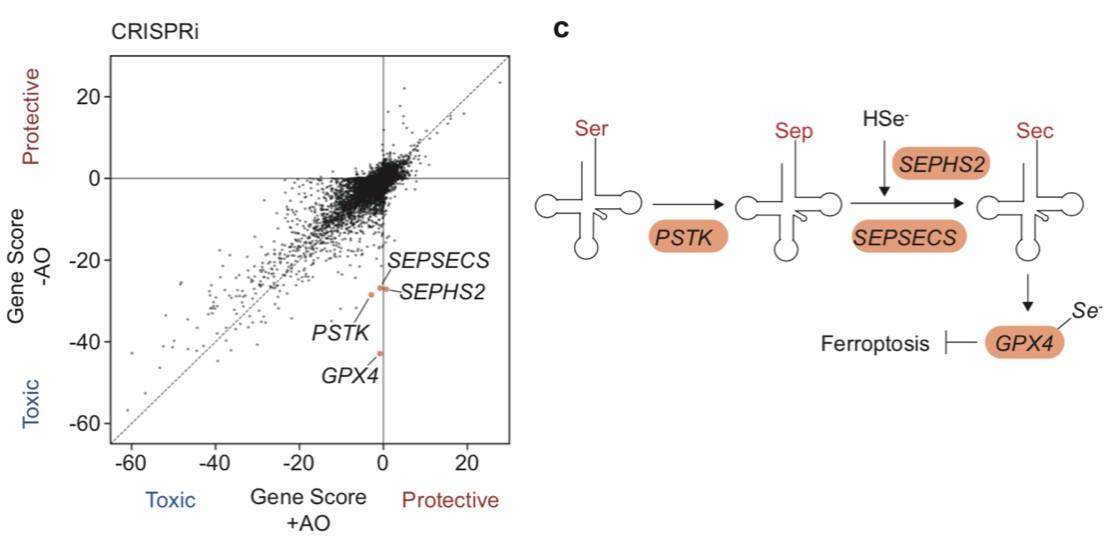
图1. 氧化应激条件下全基因组CRISPRi筛选
值得一提的是,与其他研究中经常使用强ROS诱导剂(如H2O2或rotenone)不同,该研究中作者通过去除培养液中抗氧化因子的方式,创造了更加接近生理条件的温和的慢行氧化应激刺激。筛选结果显示,铁死亡抑制因子GPX4及GPX4合成通路上的基因是神经元在氧化应激刺激条件下生存所必需的,而在正常条件下敲低这些基因没有表型,说明在氧化应激条件下神经元倾向于发生铁死亡 (图1)。
接着,为了找到神经元中直接调控ROS稳态的基因,作者分别使用可以表征细胞内ROS水平和脂质氧化水平的荧光指示剂进行了基于流式分选的全基因组筛选。有意思的是,除了已知的一些可以调控ROS的基因外,筛选还鉴定出了许多新的影响ROS稳态的基因,包括PSAP. PSAP编码蛋白prosaposin, 它定位在溶酶体中,参与糖鞘脂(glycosphingolipids)的降解。一个溶酶体蛋白如何参与ROS调控?团队对其背后的机制进行了深入的探究。
通过脂质组学分析,PSAP敲除后的神经元有大量糖鞘脂积累。意外的是,当将PSAP敲除的神经元培养在去除了抗氧化因子的培养液中,十几天后细胞全部死亡,而正常神经元仍然存活。且PSAP敲除神经元的死亡不能被细胞凋亡(apoptosis)抑制剂挽救,却能被铁死亡抑制剂完全挽救,说明PSAP缺失引发神经元铁死亡(ferroptosis)。
团队还进一步发现PSAP敲除引发溶酶体脂质代谢紊乱,导致脂褐质(lipofuscin)的形成。脂褐质中累积了许多活性的Fe2+, 通过Fenton反应生成ROS,导致脂质氧化,引起神经元铁死亡(图2)。有意思的是,这条PSAP敲除导致铁死亡的通路是神经元特异的,在HEK293, iPSC以及iPSC分化的神经干细胞和神经胶质细胞中均没有发现上述表型。
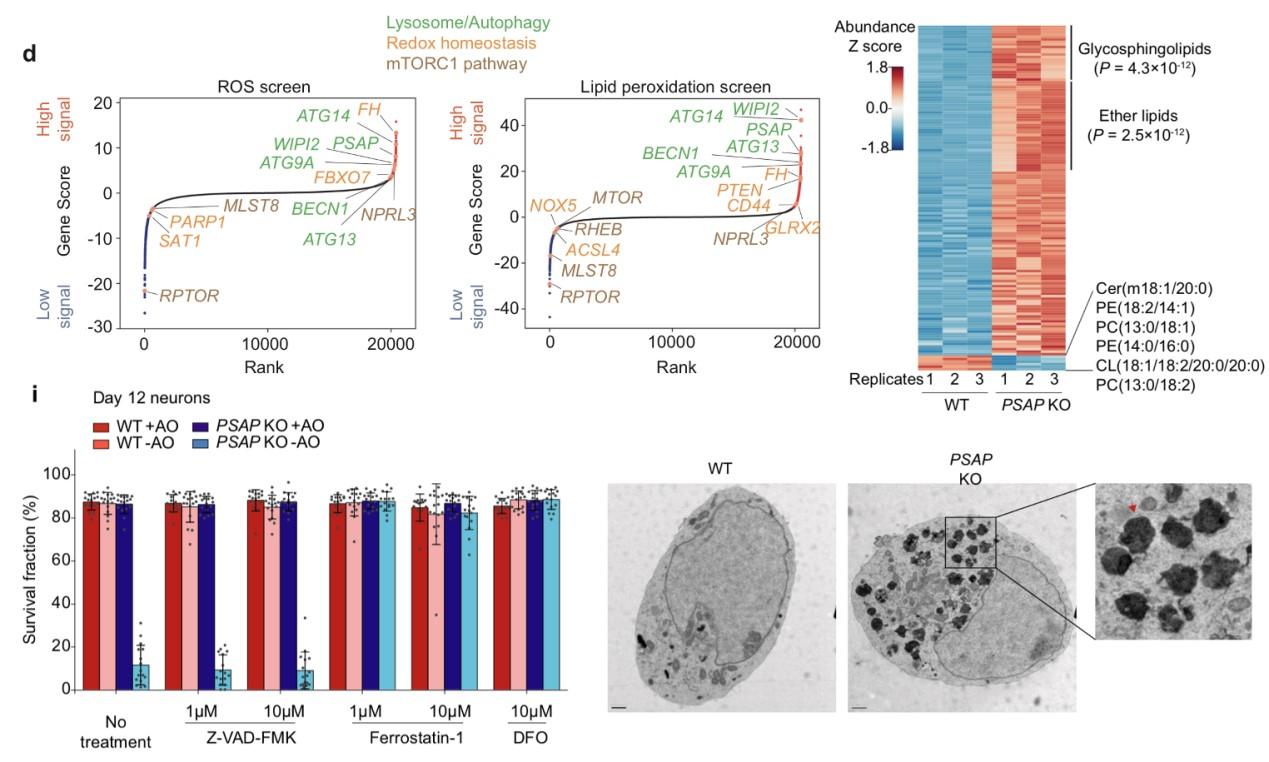
图2. PSAP缺失引起神经元铁死亡
这项研究通过大规模CRISPR筛选系统研究了神经元氧化应激的调控,阐明了由PSAP参与的溶酶体脂质代谢紊乱引发神经元铁死亡的新机制(图3)。值得注意的是,临床研究发现PSAP基因突变可以导致帕金森症,且病人大脑样本中也发现与本研究类似的表型。同时,许多神经退行性疾的病患者发生退变的脑区也发现大量铁的积累,暗示铁死亡可能是神经退行性疾病中引起神经元丧失的一个重要机制,因此抑制神经元铁死亡有可能干预神经退行性疾病的进展。
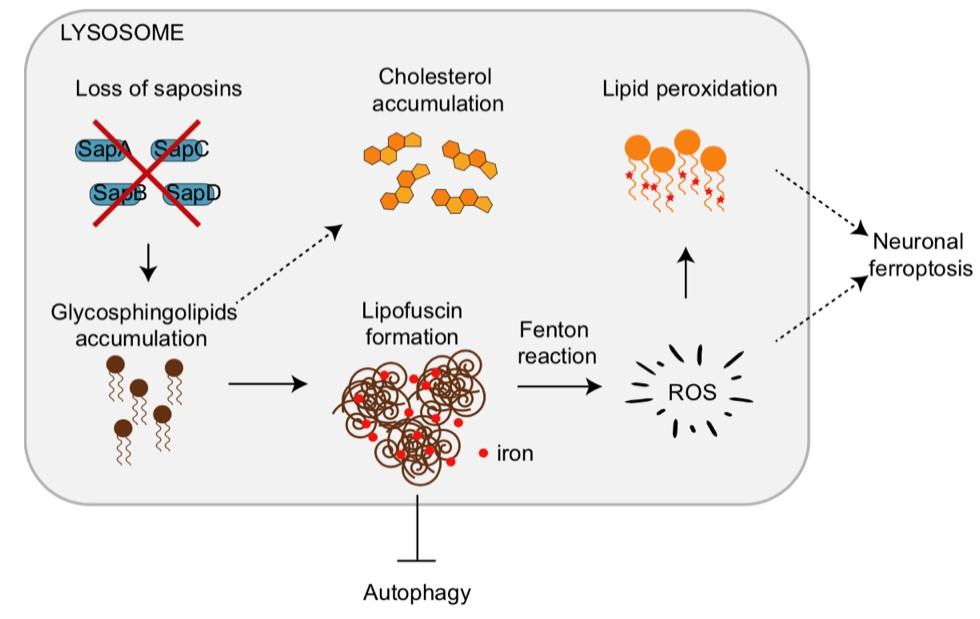
图3. PSAP缺失引起神经元铁死亡机制示意图
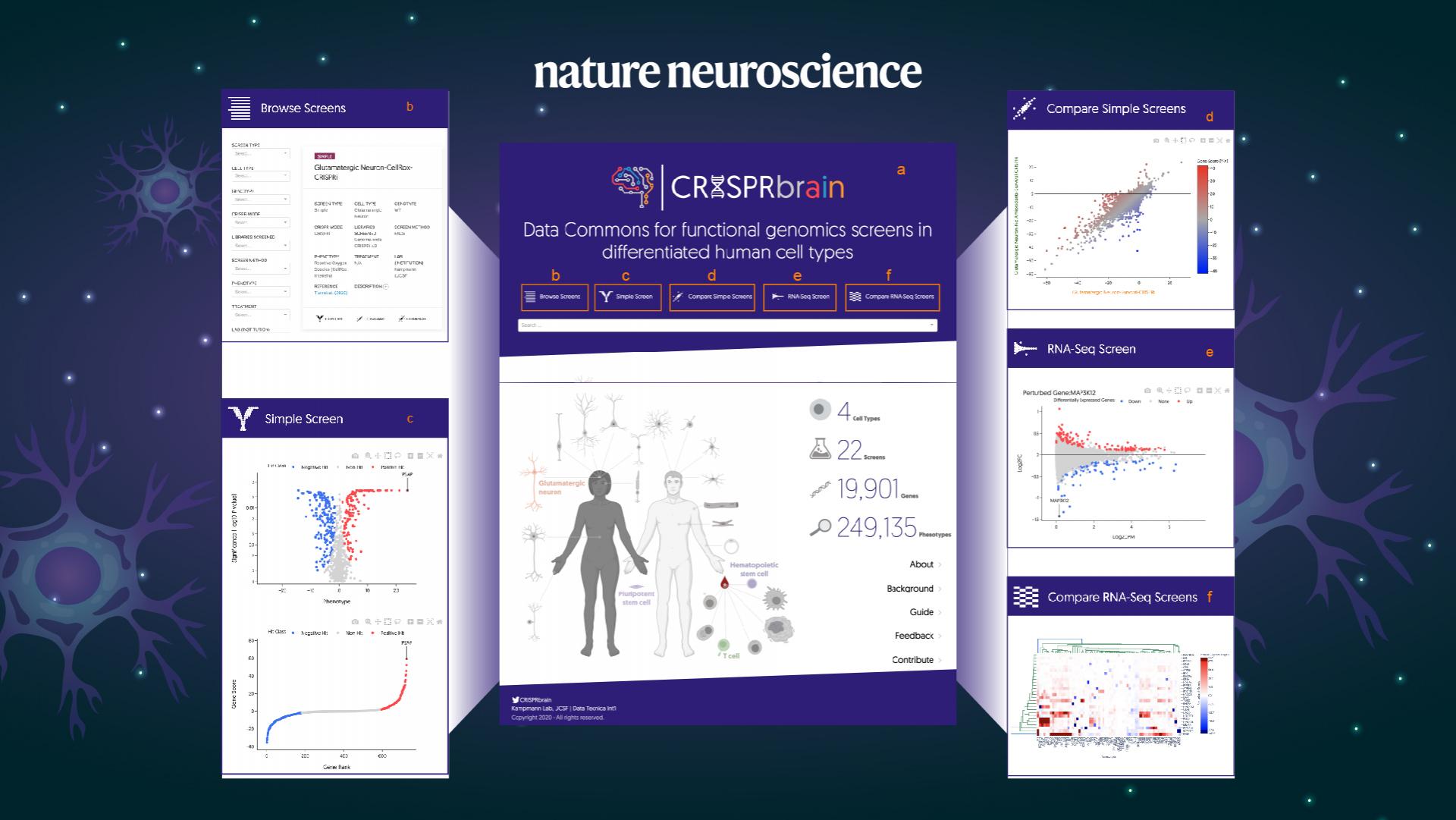
此外,这项研究还有其他重要的贡献。技术上,团队开发了在iPSC分化神经元中可诱导的CRISPRa系统,与之前的CRISPRi互补,实现了在人类神经元中全基因组的过表达筛选。数据资源上,本研究首次完成了在人类神经元中对多种表型的全基因组筛选,团队构建了CRISPRbrain数据库网站(http://crisprbrain.org/),包含了不同细胞类型和细胞表型(基于存活、荧光信号或单细胞转录组的表型)的筛选结果,便于研究者探索感兴趣基因的功能。
该研究中,田瑞琳为第一作者,与美国加州大学旧金山分校Martin Kampmann为共同通讯作者。南科大为第一单位。
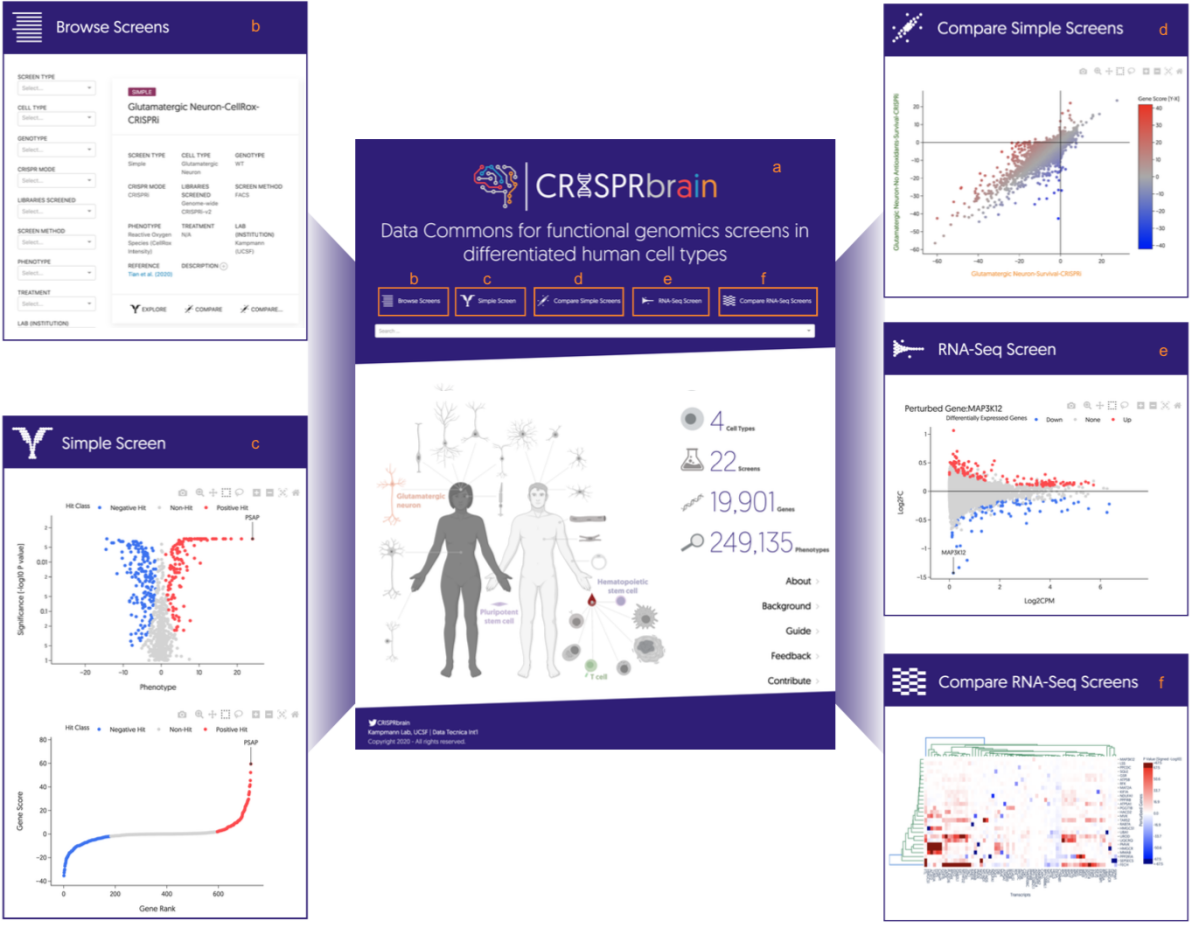
图4. CRISPRbrain 数据库网站
论文链接:https://doi.org/10.1038/s41593-021-00862-0
供稿单位:医学院
通讯员:伍渊
编辑:劳湘雯